PART 0-热学总概
## 热运动
①微观粒子的运动(至于为啥与热有关,咱也布吉岛。我jio得吧,宏观物体并不会处于永恒的、杂乱无章的运动,你给他们加热啊啥的,变话并不明显)
②包含了机械运动:几个粒子的运动遵循力学的规律,但如果是有很多粒子,每个粒子之间会相互作用,这时如果再但看一个粒子的话,会很混乱,但是,如果整体来看,大量粒子的运动却遵循一定统计规律
## 热学
研究分子热运动和其他形式运动相互转化时遵循的规律
##方法
①热力学方法:不考虑物质的微观结构,从宏观角度研究,研究热血性质&&过程的方向和限度
②统计物理方法:从微观出发,求出大量粒子的微观量的平均统计值
PART 1-平衡态 理想气体状态方程 && PART 2-准静态过程

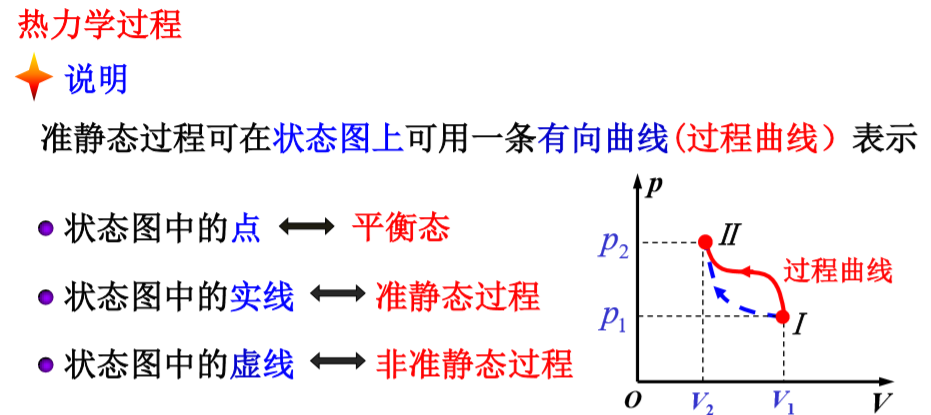
准静态过程:系统的状态变化进行的很慢很慢很慢(比闪电还慢呦),每一个状态都可以近似看成平衡态


PART 3-热力学第一定律
3.1 热力学第一定律
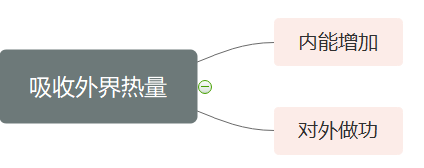
Q=E2-E1+W ↔ dQ=dE+dW

3.2 理想气体的内能
3.2.1 焦耳定律:理想气体的内能只与温度有关
3.2.2 计算


热容C:系统在某一过程中温度升高 (或降低)1 K 所吸收 (或放出)的热量
等体摩尔热容Cv:1mol理想气体在等体过程中升高单位温度所吸收的热量

等压摩尔热容Cp:1mol理想气体在等压过程中升高单位温度所吸收的热量

γmol理想气体在某一热力学过程中内能的变化量:
(内能是状态量,与过程无关,所以,只要是初末态温度为T1,T2时才可以)

3.3 热力学第一定律对理想气体的应用

■等体升压过程中气体吸收的热量,全部用来增加自身内能,使其温度上升
■等压过程吸收的热量,一部分用来做功,其余部分则用来增加其内能。
★1mol 理想气体温度升高1K时,等压过程要比等体过程 多吸收8.31J的热量,用于对外作功
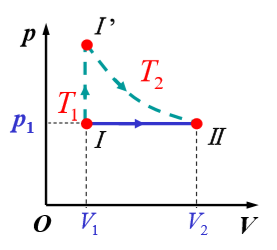
Ⅰ到Ⅰ`是和等体升压一致的,不一样的就是从Ⅰ到Ⅱ这一阶段
■在等温膨胀过程中 ,理想气体吸收的热量全部用来对外做功;
在等温压缩中,外界对气体所的功,转化为气体向外界放出的热量。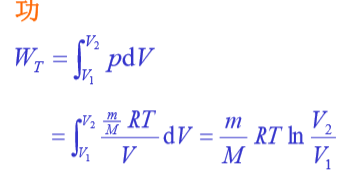
(就是p-V图里的面积)

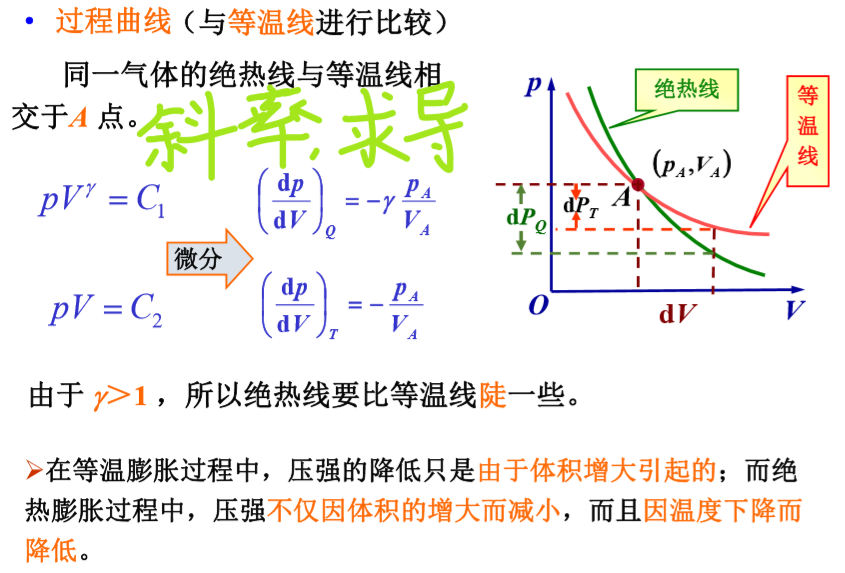
自然界及日常生活中的绝热过程
① 绝热冷却
如压缩空气从喷嘴急速喷出时,气体绝热膨胀,使气 体温度降低,甚至液化。
② 降雨
地面气团受热↑,高空气团因冷↓,形成垂直气流;
因空气传热性能差,该一过程可近似为绝热过程;
——上升热气流因绝热膨胀而降温,使饱和蒸汽压减小,
达到一定程度时,水蒸气饱和,开始凝结,并形成降雨。
==一些栗子==
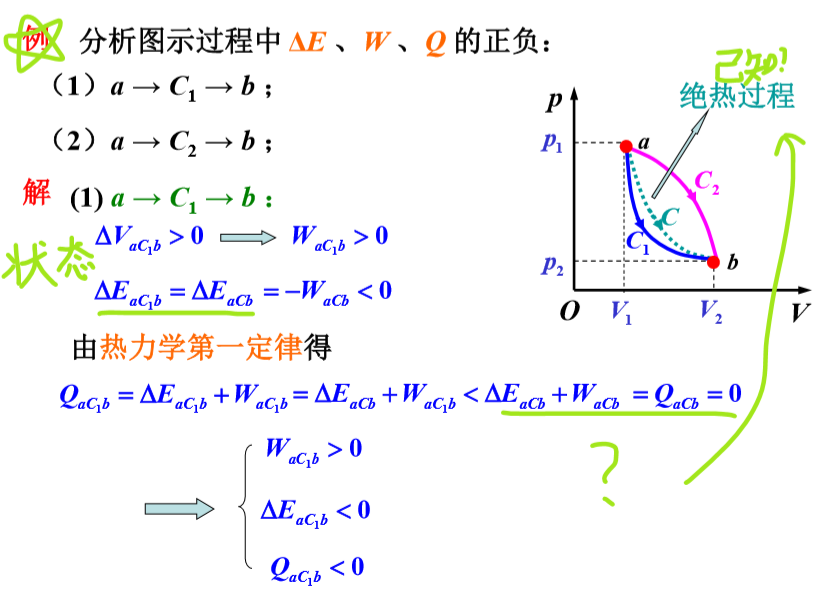
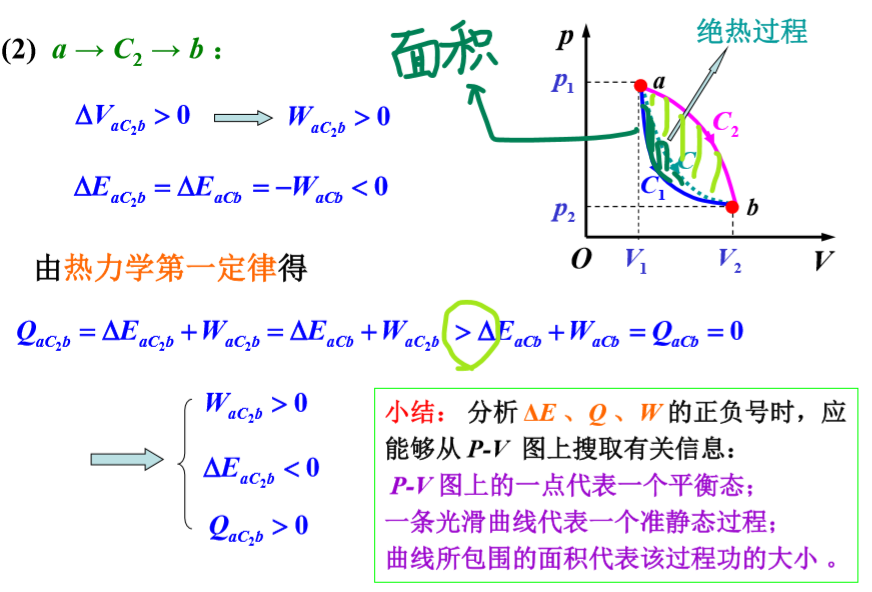
## 如果有活塞的话,要注意可以用左边求右边,右边求左边

